臨床研究など
- [公開日:2020年3月24日]
- [更新日:2025年4月3日]
- ID:148
ソーシャルサイトへのリンクは別ウィンドウで開きます
逆流性食道炎の実態と危険因子に関する検討(倫理審査委員会 承認受付番号1)
近年、日本人の食生活の変化や、慢性胃炎の原因となるヘリコバクター・ピロリ菌感染率の低下とその除菌治療の普及により、胃酸分泌能が増加しており、その結果、胃酸が食道に逆流し、胸やけなどの症状を呈する逆流性食道炎が増加してきています。高齢化率の高い南和地域では、逆流性食道炎による食道粘膜傷害のため出血をきたすような重症例も多く、その危険因子を検討し、適切な治療を行うことは重要であります。
当科では、2011年4月~2015年10月に、当院の前身である奈良県立五條病院にて施行された上部消化管内視鏡検査にて、逆流性食道炎を認めた患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センターの倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000
担当者
辻 裕樹、沢井 正佳
低用量アスピリンによる消化管障害の実態と危険因子に関する検討(倫理審査委員会 承認受付番号3)
近年、高齢者社会に伴い虚血性心疾患や脳血管障害の一次および二次予防のために低用量アスピリン(以下、LDA)服用患者が増加し、LDAによる消化管粘膜障害(びらん、潰瘍、出血)例が増加しています。上部(胃、十二指腸)消化管出血の危険因子として、高齢者、潰瘍既往、非ステロイド系抗炎症剤(NSAIDs)やワルファリンなどの抗血栓剤やステロイド剤の併用などが報告されていますが、NSAIDsと比較して、本邦でのLDAについてのエビデンスは少なく、小腸や下部(大腸)消化管出血についてはさらにエビデンスが少ないのが現状であります。
当科では、当院でアスピリン(NSAIDsや抗血栓剤併用)を投与され、消化管内視鏡(上部・下部・小腸)検査を施行された患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センター医の倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
沢井 正佳
急性胆管炎、閉塞性黄疸に対する内視鏡的治療の実態と危険因子に関する検討の後ろ向き単施設研究(倫理審査委員会 承認受付番号4)
今日、急性胆管炎や閉塞性黄疸の治療においては、EBD(内視鏡的胆道ドレナージ)が推奨され一般化しております。胆管炎や閉塞性黄疸の原因として、結石、悪性腫瘍、硬化性胆管炎などがあり、EST(内視鏡的乳頭括約筋切開術)やEP(L)BD(内視鏡的乳頭(大口径)バルーン拡張術)での截石治療やEMS(内視鏡的メタリックステント)留置術での悪性胆道狭窄疾患に対し行われ有効性が示されていますが、一定の割合で重篤な偶発症も発生しているのも事実であります。また、近年高齢化社会に伴い高齢者に対しての治療も増加し、加齢に伴う臓器能の低下や基礎疾患を併存していることも多く、術中・術後の偶発症の発生が懸念されます。ERCP(内視鏡的逆行性胆管膵管造影)関連手技であるEBDや原因治療(EST、EP(L)BD、その他)の偶発症やその対策、長期予後を検討することは重要であり、特に高齢者において検討した報告は少なく、有意義であると思われます。当科では、急性胆管炎や閉塞性黄疸に対する内視鏡的検査や治療を施行された患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センター医の倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
沢井 正佳
酸関連疾患(胃・十二指腸潰瘍、NSAIDs潰瘍、胃食道逆流症)の実態と危険因子に関する検討(倫理審査委員会 承認受付番号5)
近年、日本人の食生活の変化や、慢性胃炎や消化性潰瘍の原因となるヘリコバクター・ピロリ菌感染率の低下とその除菌治療の普及により、胃酸分泌能が増加しており、その結果として胃酸が食道に逆流し、胸やけなどの症状を呈する胃食道逆流症(GERD)が増加してきております。また、高齢化社会に伴い整形外科領域でのNSAIDs投与、あるいは脳・心血管疾患に対する低用量アスピリン(LDA)やワルファリンなどの抗血栓剤の投与が増加しており、これらの薬剤に起因する消化性潰瘍は今後ますます増加することが予測されます。これら酸関連疾患(胃・十二指腸潰瘍、NSAIDs潰瘍、胃食道逆流症)による消化管粘膜傷害のため出血、狭窄、穿孔などをきたすような重篤な症例もみられ、その危険因子を検討し、適切な治療や予防を行うことは重要であると考えます。本研究は酸関連疾患(胃・十二指腸潰瘍、NSAIDs潰瘍、胃食道逆流症)の実態と出血などの危険因子を同定することにより、これらの予防や対策に寄与することを目的としており、臨床上極めて有意義であると考えております。
当科では、当院および前進である県立五條病院で上部消化管内視鏡検査・治療を施行された酸関連疾患(胃・十二指腸潰瘍、NSAIDs潰瘍、胃食道逆流症)患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。本研究は、すでに行われた治療や診療情報を振り返って検討するものであり、患者さんに対して治療の介入を行うものではありません。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センター医の倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
沢井正佳
上部消化管出血の実態と危険因子に関する検討(倫理審査委員会 承認受付番号6)
非ステロイド系抗炎症薬(NSAIDs)や低用量アスピリン(LDA)をはじめ、抗血栓薬服用による消化管粘膜傷害は自覚症状に乏しく、突然、出血や穿孔などの重篤な症状をきたすことが臨床上大きな問題となります。本邦では、高齢化社会を迎えるにあたり、これらの薬剤を服用する患者数の増加が見込まれ、重篤な消化管出血の増加が予想されます。本研究は上部消化管出血の危険因子を同定することにより、これらの予防や対策に寄与することを目的としており、臨床上極めて有意義であると考えております。
当科では、当院および前進である県立五條病院で吐血や黒色便を主訴に、緊急上部消化管内視鏡検査・治療を施行された患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。本研究は、すでに行われた治療や診療情報を振り返って検討するものであり、患者さんに対して治療の介入を行うものではありません。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センター医の倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
岩井聡始、沢井正佳
PEGの現状と適応および摂食不良患者に対する摂食嚥下機能療法の現状と意義(倫理審査委員会 承認受付番号7)
日本は超高齢化社会を迎え、脳血管疾患や認知症などにより経口摂取困難となる例が増加しています。それを背景に経皮内視鏡的胃瘻造設術(PEG)は近年急速に普及し、経口摂取不能の患者に対して栄養状態の改善をもたらし多大な効果が得られるようになりました。胃瘻からの栄養剤の適切な投与により、栄養状態が改善し嚥下訓練が進み経口摂取が再開されるようになった症例もしばしば経験されます。しかし一方で近年のマスコミ報道などによるPEGのマイナスイメージのため、PEG=終末期、延命治療といった誤解が生じている面もあります。そのため医学的な観点からのPEG造設の適応、摂食嚥下機能療法の意義を検討することは、臨床上極めて有意義であると考えています。
当科では、PEG造設をされた患者さん、摂食嚥下機能療法を受けられた患者さんの臨床経過を診療記録より過去にさかのぼって調査を行い検討させて頂くこととなりました。本研究は、すでに行われた治療や診療情報を振り返って検討するものであり、患者さんに対して治療の介入を行うものではありません。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センターの倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
堀内葉月、沢井正佳
下部消化管出血の実態と危険因子に関する検討の後ろ向き単施設研究(倫理審査委員会 承認受付番号12)
下部消化管出血を来す疾患は自覚症状に乏しく、突然、出血性ショックや敗血症、消化管狭窄・穿孔などの重篤な症状をきたすことが臨床上大きな問題であることが知られています。本邦では、すでに高齢化社会を迎えており、抗血栓剤服用率の増加などからもこれらの下部消化管出血を来す疾患の増加が見込まれます。本研究は、下部消化管出血を来す疾患および患者背景を明らかにすることにより、出血の予防や治療に寄与することを目的とし、臨床上極めて有意義であると考えております。
今回当科では、当院で血便を主訴に、緊急下部消化管内視鏡検査・治療を施行された患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。本研究は、すでに行われた治療や診療情報を振り返って検討するものであり、患者さんに対して治療の介入を行うものではありません。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センター医の倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
沢井正佳
膵臓癌診断・治療標的の探索を目的とした残余液状検体からの遺伝子変異検査の検討(倫理審査委員会 承認受付番号31)
このたび、あなたには、私どもの研究「膵臓癌診断・治療標的の探索を目的とした残余液状検体からの遺伝子変異検査の検討」にご参加いただきたく、お願い申し上げます。この研究はあなたの組織から「DNA」を抽出して解析することを通じ、病気の原因を究明し、治療に役立てることを目指すものです。「DNA」とは、人間の身体を作る設計図にあたるものです。人間の身体は、約37兆個の細胞からなっていますが、遺伝子は、細胞一つ一つの中の「核」という部分に入っています。人間の身体は、この遺伝子の働きに基づいて成長し、維持されています。また、遺伝子の働きは病気にも関係しています。これまでに、遺伝子の働きから病気の原因を調べる研究が進められてきましたが、未だ原因を解明できていない病気が数多くあります。
近年、技術革新が進んだことで、一つの遺伝子ではなく、ヒト一人が持つ複数の遺伝情報と病気との関わりについて調べることができるようになりました。これによって、これまで原因を調べることが困難であった疾患についても、究明できる可能性が高まっています。
今回の研究は患者さんに侵襲のない、EUS-FNAの残余液状検体を用いて次世代シーケンサーを用いた複数のがん関連遺伝子の解析がどの程度可能かを明らかにすることを目的としています。
この研究は、倫理審査委員会で審査・承認され、研究機関の長の許可を受けたものです。この研究にご協力いただくかどうかは、あなたの自由意思に委ねられています。
研究にご協力頂けない場合でも、あなたに不利益はありません。また、研究に参加された後に同意を撤回することも可能です。この場合でも、あなたにとって不利益が生じることは一切ありません。
もし同意を撤回される場合は、同意撤回書に記入し、末尾のお問い合わせ先へご連絡ください。同意撤回書を提出された場合、基本的には試料・情報は破棄します。しかし、研究成果が論文や学会などで発表された場合は、同意を撤回されても論文や学会で発表された内容を取り下げることはできません。公的データベースから個人毎のデータが公開されている場合は、原則、あなたのデータをデータベースから削除し、その後の研究に提供しないようにデータベース側に要請します。ただし、あなたのデータを特定できない場合は破棄できない可能性があります。
不明な点があれば説明者にお尋ねいただくか、末尾のお問い合わせ先までご連絡ください。
南奈良総合医療センター消化器内科を受診された患者さまへ
当科では下記の臨床研究を奈良県立医科大学と共同で実施しております。
本研究の対象者に該当する可能性のある方で診療情報等を研究目的に利用または提供されることを希望されない場合は、下記に問い合わせてください。
本研究は、南和広域医療企業団 南奈良総合医療センターの倫理審査委員会の承認を受け、院長の許可を得て実施されます。
研究課題名
膵臓癌診断・治療標的の探索を目的とした残余液状検体からの遺伝子変異検査の検討
研究責任者
沢井 正佳(南奈良総合医療センター消化器内科・部長)
共同研究者
畠山金太(奈良県立医科大学病理部・病理診断学講座 准教授)
美登路 昭(奈良県立医科大学消化器・内分泌代謝内科・准教授)
吉治 仁志(奈良県立医科大学消化器・内分泌代謝内科・教授)
庄 雅之(奈良県立医科大学消化器・総合外科・教授)
本研究の目的
画像所見で腫瘤が発見され膵臓がんが疑われる場合、本院では超音波内視鏡下穿刺吸引法EUS-FNA (Endoscopic UltraSound-guided Fine Needle Aspiration)を用いて病理診断が行われています。今回の研究は、この病理診断に使用したEUS-FNA標本の残余を用いて、複数のがん遺伝子の解析がどの程度可能かを検討する研究です。複数のがん遺伝子の変異を明らかにすることで、今後形態で判断が難しい症例でも良悪の診断が可能になる可能性、予後予測につながる可能性、治療可能な因子を探索できる可能性があります。
該当期間
2018年12月1日~2020年12月31日
研究期間
倫理審査委員会承認後~2021年3月31日
対象となる患者さま
上記期間内に南和広域医療企業団 南奈良総合医療センターにてEUS-FNA検査を受けた患者さま
取り扱うデータ
年齢、性別、画像所見、臨床・病理診断、遺伝子変異検査結果
個人情報の取り扱い
利用する情報から氏名や住所等の患者さまを直接特定できる個人情報は削除致します。また、研究成果は学会等で発表を予定していますが、その際も患者さまを特定できる個人情報は利用しません。
患者さまの個人情報は消化器内科の沢井正佳が厳重に管理します。
利益相反
本研究に関連し開示すべき利益相反関係にある企業等はありません。
お問い合わせ先
相談窓口:消化器内科
担当者:沢井 正佳(部長)
電話:0747-54-5000
E mail:sawai-masayoshi@nanwairyou.jp
「進行肝細胞癌に対する分子標的薬療法に関する多施設共同研究」(倫理審査委員会 承認受付番号33)
これまでに進行肝細胞癌の治療を受けた患者さんへ
南奈良総合医療センターでは、奈良県立医科大学消化器内分泌代謝内科と共同で「進行肝細胞癌に対する分子標的薬療法に関する多施設共同研究」という臨床研究を実施しております。この研究は進行肝細胞がんに対する分子標的薬を用いた全身化学療法の有効性を調べることを主な目的としています。この臨床研究の概要についてご確認いただき、問い合わせなどがありましたら「問い合わせ先」へご照会ください。
この臨床研究は、南奈良総合医療センター倫理審査委員会で審査され、病院長の許可を得て行います。
研究責任者
南奈良総合医療センター消化器内科 沢井正佳
研究の目的
実臨床における全身化学療法の有効性を多施設共同で検証します。
研究期間
研究の対象となる期間:2018年3月1日~2024年12月31日
全体の研究期間:倫理審査承認日~2027年12月31日
研究の方法
進行肝細胞がんに対して、全身化学療法の投薬を受け治療された患者さんに対し、患者背景(性別や年齢、肝疾患の原因など)や腫瘍の大きさ・個数・腫瘍マーカーといった腫瘍に関する情報、肝機能などの血液データ、また投薬治療後の治療効果に関するデータを収集し解析します。(収集するデータは、治療開始前、治療開始後1ヶ月、3ヶ月、6ヶ月、12ヶ月、24ヶ月後が対象です。)
個人情報の取扱い
カルテIDや氏名などの個人情報を研究用IDに置きかえて使用するため、あなたの個人情報が外部へ漏れることはありません。カルテIDと研究IDの対応表は厳重に研究責任者において管理されます。
研究の成果は、学会や学術誌などで公表されますが、この場合も、個人が特定される情報が公開されることはありません。
利益相反
利益相反とは、「主に経済的な利害関係によって公正かつ適正な判断が歪められてしまうこと、または、歪められているのではないかと疑われかねない事態」のことを指します。具体的には、製薬企業等から研究者へ提供される謝金や研究費等がこれにあたります。
この研究は、奈良医大消化器内分泌代謝内科の研究費で実施します。特定の企業・団体等からの支援を得て実施するものではありません。
「消化器内視鏡に関連する疾患、治療手技データベース構築(多施設共同 前向き観察研究)」(倫理審査委員会 承認受付番号34)
当院で内視鏡検査治療を受けられる方へ
現在、日本消化器内視鏡学会では以下の臨床研究を実施しています。当院では、この研究の一部を分担しています。
この研究は、日本全国の消化器内視鏡検査・治療情報を登録し、集計・分析することで医療の質の向上に役立て、患者さんに最善の医療を提供することを目指す研究プロジェクトです。この研究の実施に先立ち、研究実施者は倫理審査委員会において医学的必要性、研究の倫理面、安全面、妥当性の観点から審査を受け承認を得ています。
情報等の使用について、直接に説明して同意はいただかずに、このお知らせをもって研究に関する事項を公開いたします。対象となる方におかれましては、研究の主旨・方法をご理解いただきますようお願い申し上げます。
この研究への参加(試料・情報提供)を希望されない場合、あるいは、研究に関するご質問は下記の問い合わせ先へご連絡ください。
研究期間は 2015年1月1日~2028年12月31日です。
研究課題名
「消化器内視鏡に関連する疾患、治療手技データベース構築12版 (ver.12.0)」
当院での研究対象者
2018年1月より2028年12月までに南奈良総合医療センターにおいて内視鏡検査・治療を受けた方
1.情報の利用目的および利用方法
この研究は、日本消化器内視鏡学会内に設けられたJapan Endoscopy Database(JED) Project 委員会が主導となり企画された多施設共同研究です。当初は、東京大学医学部附属病院、国立がん研究センター中央病院、北里大学病院、虎の門病院、京都大学医学部附属病院、東京医科歯科大学医学部附属病院、東京慈恵会医科大学葛飾医療センター、埼玉医科大学国際医療センターの8 施設(共同研究機関)のみで開始いたしましたが、現在、日本全国の消化器内視鏡検査および治療情報を登録し、集計・分析することで医療の質の向上に役立て、患者さんに最善の医療を提供することを目指すプロジェクトです。この様な内視鏡関連手技の全国規模の情報集積は初めてのこころみであり、患者側だけでなく、医療を提供する側にも大きな利益をもたらすものと考えています。
その為に、内視鏡部門システムから以下に記載する項目を抽出し、個人が特定できない状態(匿名化)で日本消化器内視鏡学会に提供され、学会本部に設置したサーバ内に格納しデータベースを構築し、各種分析が行われます。
日本消化器内視鏡学会では、この研究で集められたデータを分析することで以下のことを明らかにすることを目的にしています。
●内視鏡関連手技を行っている施設診療科の特徴
●医療水準の評価
●適正な消化器内視鏡専門医の配置、ならびに消化器内視鏡技師、看護師などのコメディカルの適正な配置
●早期癌登録に対する精確な情報収集
●内視鏡検査、治療を受けた方の予後
●内視鏡検査・治療の医療経済的な情報収集
●これから内視鏡関連手技を受ける方の死亡・合併症の危険性,など
この研究成果は学会発表、学術雑誌およびデータベースなどで公表します。
本研究に登録されたデータを利用して、上記に記載されていない解析等を行い研究を実施する場合は、その都度日本消化器内視鏡学会の倫理委員会で科学性、倫理性、研究の意義、個人情報保護の観点から審査され可否が決定されます。
2.利用し、または提供する情報の項目
検査日、年齢、性別、ASA Grade、抗血栓薬(使用状況ならびに中止、置換の有無などの詳細)、喫煙歴ならびに喫煙の有無、飲酒歴および飲酒状況、悪性腫瘍、家族歴、他臓器癌既往歴、ヘリコバクター・ピロリ感染状態、内視鏡検査の予定性、外来・入院、検査目的、治療目的、鎮痙剤使用状況、鎮静・鎮痛・麻酔に関する事項、内視鏡の挿入経路、使用スコープ情報、送気の種類、特殊観察法、観察範囲、手技開始・終了時間、手技中、手技後偶発症、30日以内の死亡の有無、実施医師名、副実施医師名、内視鏡看護師・技師名、腹部手術歴、生涯大腸内視鏡歴、
造影範囲、挿管、胆管・膵管径、挿管難易度、胆管へのアプローチ方法 、など
3.利用する者の範囲(データを使って解析等を行う研究機関・研究者等)
研究の実施体制(多施設共同研究)
統括責任者:日本消化器内視鏡学会Japan Endoscopy Database (JED) Project委員会 委員長 田中 聖人
研究事務局 日本消化器内視鏡学会 事務局
共同研究機関および研究責任者:
東京大学医学部附属病院 藤城光弘
国立がん研究センター中央病院 斎藤豊
北里大学病院 木田光広/堅田親利
虎の門病院 布袋屋修
京都大学医学部附属病院 武藤学/堀松高博
東京医科歯科大学医学部附属病院 大塚和朗
東京慈恵会医科大学葛飾医療センター 加藤正之
埼玉医科大学国際医療センター 良沢昭銘
南奈良総合医療センター 沢井正佳
研究協力機関(情報を提供のみを行う機関):別添資料2
4.情報の管理について責任を有する者の氏名または名称
統括責任者:日本消化器内視鏡学会Japan Endoscopy Database (JED) Project委員会 委員長 田中 聖人
当院の研究責任者:南奈良総合医療センター 沢井正佳
5.研究対象者またはその代理人の求めに応じて、研究対象者が識別される情報の利用または他の研究機関への提供を停止すること
研究対象者となる方または代理の方で、本研究への情報の利用にご賛同頂けない場合は、情報の利用を停止することができます。停止を求められる場合には下記(6)にご連絡ください。また、未成年者の場合は、研究対象者の親権者または未成年後見人が拒否できる機会を保障します。いずれの場合も利用に賛同頂けなくても、何ら不利益は生じません。
ただし、検査・治療から6ヵ月経過した情報に関しては利用させていただきます。
6.5の研究対象者またはその代理人の求めを受け付ける方法
南奈良総合医療センター 電話:0747-54-5000、内線2298(医局)、消化器内科
連絡担当者:消化器内科 沢井正佳
研究責任者:消化器内科 沢井正佳
研究主任施設:電話番号03-3525-4670、日本消化器内視鏡学会事務局・Japan Endoscopy Database(JED)Project 委員会
研究協力機関(情報を提供のみを行う機関):別添資料2
<共同研究機関一覧> 2 埼玉医科大学国際医療センター
6 広島県厚生農業協同組合連合会 廣島総合病院
7 独立行政法人 東京都健康長寿医療センター
12 独立行政法人地域医療機能推進機構 京都鞍馬口医療センター
15 医療法人五星会 菊名記念病院
35 東京医科歯科大学病院
65 藤枝市立総合病院
74 社会福祉法人恩賜財団済生会支部千葉県済生会 千葉県済生会習志野病院
82 国家公務員共済組合連合会 虎の門病院
87 独立行政法人労働者健康安全機構 関西ろうさい病院
89 国立大学法人 京都大学医学部附属病院
96 朝日大学病院
105 東京大学医学部附属病院
109 京都府公立大学法人 京都府立医科大学附属病院
110 国立大学法人 東北大学病院
125 パナソニック健康保険組合 松下記念病院
164 社会福祉法人恩賜財団 済生会有田病院
168 磐田市立総合病院
177 社会福祉法人恩賜財団済生会支部 富山県済生会富山病院
186 香川県立中央病院
204 社会医療法人財団大樹会 総合病院回生病院
231 長野県厚生農業協同組合連合会 北信総合病院
271 国立大学法人 広島大学病院
273 SUBARU健康保険組合 太田記念病院
274 国立大学法人 秋田大学医学部附属病院
278 日本赤十字社 旭川赤十字病院
284 慶應義塾大学病院
300 地方独立行政法人総合病院 国保旭中央病院
329 南和広域医療企業団 南奈良総合医療センター
333 独立行政法人地域医療機能推進機構 九州病院
334 日本赤十字社 京都第二赤十字病院
339 日本赤十字社 高松赤十字病院
360 地方独立行政法人広島市立病院機構 広島市立北部医療センター安佐市民病院
385 公益財団法人東京都医療保健協会 練馬総合病院
402 大阪公立大学医学部附属病院
注意:数字は、申請時に発番される管理番号です。
410 地方独立行政法人奈良県立病院機構 奈良県西和医療センター
417 兵庫県立西宮病院
430 静岡県立静岡がんセンター
432 兵庫医科大学
449 社会医療法人きつこう会 多根総合病院
484 社会福祉法人恩賜財団大阪府済生会吹田医療福祉センター 大阪府済生会吹田病院
514 国家公務員共済組合連合会 高松病院
541 独立行政法人国立病院機構 兵庫中央病院
581 独立行政法人国立病院機構 金沢医療センター
603 独立行政法人国立病院機構 仙台医療センター
608 旭川医科大学病院
625 国立がん研究センター中央病院
626 学校法人慈恵大学 東京慈恵会医科大学附属病院
627 学校法人慈恵大学 東京慈恵会医科大学葛飾医療センター
628 学校法人慈恵大学 東京慈恵会医科大学附属柏病院
641 公益財団法人大原記念倉敷中央医療機構 倉敷中央病院
679 日本赤十字社 福井赤十字病院
688 日本医科大学付属病院
709 秋田県厚生農業協同組合連合会 平鹿総合病院
715 独立行政法人地域医療機能推進機構 四日市羽津医療センター
729 国立大学法人 九州大学病院
763 日本赤十字社 大津赤十字病院
789 北里大学メディカルセンター
790 北里大学病院
831 学校法人昭和大学 昭和大学病院
834 独立行政法人労働者健康安全機構 大阪労災病院
835 日本赤十字社 秋田赤十字病院
896 東京医療生活協同組合新渡戸記念 中野総合病院
898 市立奈良病院
925 独立行政法人国立病院機構 岡山医療センター
936 藤田医科大学ばんたね病院
966 大垣市民病院
978 公立那賀病院
981 福井県立病院
985 関西電力株式会社 関西電力病院
1000 地方独立行政法人東京都立病院機構 東京都立多摩北部医療センター
1048 社会医療法人財団新和会 八千代病院
注意:数字は、申請時に発番される管理番号です。
1056 京都府公立大学法人 京都府立医科大学附属北部医療センター
1071 社会医療法人蘇西厚生会 松波総合病院
1075 公益財団法人慈愛会 今村総合病院
1083 日本赤十字社 小川赤十字病院
1090 社会福祉法人函館厚生院 函館五稜郭病院
1119 学校法人東京医科大学 東京医科大学八王子医療センター
1144 鳥取県立厚生病院
1191 埼玉医科大学病院
1196 岡山大学病院
1214 熊本市立熊本市民病院
1266 神戸市立医療センター中央市民病院
1304 国家公務員共済組合連合会 平塚共済病院
1315 社会医療法人 製鉄記念室蘭病院
1318 公益社団法人地域医療振興協会 東京北医療センター
1323 一宮市立市民病院
1324 独立行政法人国立病院機構 旭川医療センター
1411 大網白里市立 国保大網病院
1418 和泉市立総合医療センター
1528 東北医科薬科大学若林病院
以上、91機関
2025年2月18日更新
過疎高齢化医療圏の早期胃癌診療における内視鏡的粘膜下層剥離術(ESD)の実態と有用性の後ろ向き単施設の検討(倫理審査委員会 承認受付番号 No.35)
当院(南奈良総合医療センター)は、過疎高齢化地域である南和医療圏を担っております。南和医療圏の2015年の総人口に対する65歳以上の高齢者の割合推定は36.6%であり、全国平均26.6%に比べ高齢化率が非常に高い医療圏であります。2045年に全国平均の高齢者割合が36.8%となることが推定されており、現在の南和医療圏の医療は、30年先の医療を行っている状況とも考えられます。このような過疎高齢化地域において、早期胃癌診療における内視鏡的粘膜下層剥離術(ESD)の実態と有用性を明らかにすることは非常に興味深く、また高齢化地域医療への有益性の高い研究となりうると考えます。本研究では、南和医療圏での早期胃癌の内視鏡的粘膜下層剥離術(ESD)を受ける患者さんを対象に、治療の適応、偶発症、治療成績、長期予後に関するデータを収集・分析することで、今後超高齢化社会で問題となるであろう高齢者早期胃癌のより良い治療戦略を構築することを目的とします。
今回当科では、当院で早期胃癌にて内視鏡的粘膜下層剥離術(ESD)での治療を施行された患者さんの臨床経過を診療記録より調査を行い、後ろ向きに検討させて頂くこととなりました。本研究は、すでに行われた治療や診療情報を振り返って検討するものであり、患者さんに対して治療の介入を行うものではありません。
この研究で得られた成果を専門の学会や学術雑誌に発表する可能性があります。ただし、成果を公表する場合には、臨床データを使用させて頂いた方のプライバシーに慎重に配慮します。個人を特定できる情報が公表されることはありません。この研究は南奈良総合医療センター医の倫理委員会の審査を経て承認を得ています。これらの研究において、ご自身の提供された情報等について患者さんまたはご家族が問い合わせたい、もしくは利用を拒否したいなどの場合には下記にご連絡ください。なお、拒否されても患者さんへ診療上の不利益などは生じませんのでご安心ください。
南奈良総合医療センター 消化器内科
電話 0747-54-5000(内線2298医局)
担当者
大倉康志、沢井正佳
消化器内視鏡に関連した偶発症の全国調査(日本消化器内視鏡学会倫理審査委員会 承認受付番号 E19-001・変更(継続))
人を対象とする医学系研究に関する情報公開
このたび,日本消化器内視鏡学会倫理委員会の承認を得て、下記の人を対象とする医学系研究を実施します。関係各位のご理解とご協力をお願い申し上げます。
2020年3月19日
施設名 南奈良総合医療センター
代表者氏名 消化器内科 沢井正佳
研究課題名
消化器内視鏡に関連した偶発症の全国調査
研究期間
2020年3月(倫理委員会承認後)~2021年12月31日
研究の意義・目的
日本消化器内視鏡学会は,消化器内視鏡に関連した偶発症を1983年から5年毎に,これまで6回にわたり全国的に調査を行ってきました.6回目の調査は2008年から2012年まで行われ,その結果は2016年に本学会誌に公表されています.この実態を知ることは,安全かつ効果的な消化器内視鏡診療の遂行に欠かせないものであり,日本消化器内視鏡学会としては近年の実態についての調査が必要と考えています.
一方,これまでの5年間をまとめた調査では前方視的調査と比べて偶発症頻度にかなりの較差があることが判明しました.そのため今回の「消化器内視鏡に関連した偶発症の全国調査」では,発生した偶発症については,調査期間を短く任意設定した前向き調査,ならびに,重症事例調査として,任意に設定した調査期間の3年以内に起こった重症事例を後ろ向きに調査し,従来の調査に比してより実態に近い調査を施行することとしました.本研究では,上記の前向きおよび後ろ向きの結果を併せて検討し,消化器内視鏡に関連した偶発症の実態を明らかにする事を目的とします.
研究の方法
本研究は,各施設で任意に設定した調査期間中(1週間)に発生した,消化器内視鏡に関連した偶発症((1)術者側の事故数,(2)前処置と感染に関する偶発症発生数,(3)消化器内視鏡の検査総数および偶発症発生数(生検を含む観察のみ),(4)内視鏡治療の実施例数および偶発症発生数,(5)腹腔鏡における検査および治療総数と偶発症発生数(外科治療を除く),および,発生した偶発症の詳細についてケースカードに入力し,データを収集します.また,任意に設定した期間から遡って3年以内に発生した重症事例についても調査します.なお,データについては日本消化器内視鏡学会で集約し,解析の上公表いたしますが,個々人の情報別に示されることはありません.
調査期間は,2019年4月1日から2021年6月30日の任意の1週間とします.また,重症事例の調査は,設定した1週間から遡った3年間を調査期間といたします.
研究組織
研究実施医療機関
- 日本消化器内視鏡学会医療安全委員会
- 研究代表責任者
日本消化器内視鏡学会 医療安全委員会 担当理事 入澤篤志
獨協医科大学医学部 内科学(消化器)講座 主任教授 - データ登録・管理
浜松医科大学臨床研究センター 古田隆久
本研究に関する問い合わせ先
本研究に関する御質問等がございましたら、下記の連絡先まで問い合わせてください。他の研究対象者等の個人情報および知的財産の保護等に支障がない範囲内で研究計画書および研究の方法に関する資料を閲覧できます。
また、試料・情報が当該研究に用いられることについて研究対象者ご本人または代理人の方に御了承いただけない場合には、研究対象者とはせずに試料・情報の利用、提供をいたしませんので、下記の連絡先までお申し出ください。その場合でも研究対象者ご本人または代理人の方に不利益が生じることはありません。なお、研究結果が既に医学雑誌への掲載や学会発表がなされている場合、データを取り消すことは困難な場合もあります。
- 研究内容に関する問い合わせの窓口
機関名:南奈良総合医療センター
事務担当者:消化器内科 沢井正佳 - 試料・情報を当該研究に用いられることについて拒否する場合の連絡先
各施設の問い合わせ窓口
機関名:南奈良総合医療センター
事務担当者:消化器内科 沢井正佳
アルコール性肝障害/依存症を有する患者に対するナルメフェンの飲酒量低減治療後の肝機能の推移(倫理審査委員会 承認受付番号 A6)
1. 臨床研究について
「臨床研究」というのは耳慣れない言葉ですが、ある薬剤や治療法が人の特定の病気に対して有効かどうか、また安全かどうか、実際に患者さんにご協力いただいて研究することをいいます。また現在使われている薬でも、適応疾患への効果とは別の相乗効果、その安全性を調べることもあります。多くの場合、特定の病気に対して、効果および副作用などを総合的に判定し、どの治療法が有効なのかを評価します。ここでより有効とわかった治療法がその後の一般的な治療法となりえます。新しい治療法や新しい薬が必ずしも良いとは限らないため、このような研究を行って慎重に検討していきます。
2. 臨床研究への参加について
現在、私達はアルコール性肝疾患を抱える患者さんのより良い治療法を調べるための臨床研究を行なっています。今回あなたの病状が、今から説明する『アルコール性肝障害/依存症を有する患者に対するナルメフェンの飲酒量低減治療後の肝機能の推移』の参加基準にあてはまっているため、参加していただけるかどうかお伺いをしています。この臨床研究にご参加いただくかどうかはあなたの意思を尊重いたします。参加を希望されない場合は、遠慮なくその旨をお知らせください。また、研究参加に同意された後でも、いつでもこれをやめることができます。なお、お断りになられたからといって、気まずくなったり、治療が受けられなくなったりするなどの不利益を受けることは一切ありません。これからこの研究の内容について私(担当医師)からの説明を聞き十分に理解していただいたうえでこの研究にご協力いただけるかどうかあなたのご意思でお決めください。この説明文の中でわからない言葉や表現、疑問な点があればチェックしておいて、私(担当医師)に質問してください。また、説明の中でわからないことがあれば、どんなことでも、遠慮せずに私(担当医師)に何回でも質問してください。また、あなたの希望により他の患者さんの個人情報保護やこの研究の独創性の確保に支障がない範囲内で、研究計画および研究の方法に関する資料等を入手または閲覧することができます。
3. 同意について
あなたがこの臨床研究に参加してくださるかどうかは、私(担当医師)による説明のあった以降にうかがいます。臨床研究に参加してくださる場合は、口頭にて同意の意思を示していただきます。説明後この説明文書はお渡ししますので、よく読んでご検討いただければ幸いです。
4. あなたの病気について
あなたの病気はアルコール性肝障害およびアルコール依存症と考えられます。アルコール性肝疾患は禁酒が治療の基本となりますが、アルコール常飲者の断酒には難渋することが多いとされています。アルコール性肝障害をもつ患者さんがアルコール摂取を継続した場合、肝の炎症、腸内細菌異常増殖、腸管粘膜のバリア機能低下、アセトアルデヒド(アルコールの代謝物質)による線維化誘発細胞の活性化などにより肝線維化が進行し、肝硬変へ進行することが予想されます。肝硬変への進行を抑えるためには禁酒が必要です。断酒が困難な場合、近年、中間目標として飲酒量を減らすことで飲酒による害を軽減するという概念(ハームリダクション)が提唱されています。肝硬変診療ガイドライン第3版において、アルコール性肝硬変患者に対するハームリダクションの効果に関して検討が必要であることが記載されてもあり、アルコール性肝障害の患者さんに対してナルメフェンが治療の選択肢になるのではないかと考えられています。
5. この臨床研究の目的
アルコール性肝疾患の治療の根幹となるのは断酒です。断酒がどうしても困難な場合に、ハームリダクションの考えに則り、アルコール性肝障害を有する患者さんにナルメフェンを投与した場合に、飲酒量の変化、肝機能、線維化マーカー、などに改善効果が実際にみられるかどうかを検討することが今回の研究の目的です。
6. 臨床研究の内容
1)研究期間
実施承認後~2026年12月31日
2)検査および観察項目
ナルメフェンの内服開始時内服後 1 か月目、同 3 か月目、同 6か月目、同 12 か月目に通常の診療で行う一般診察と血液検査、問診の下記の項目を、この臨床研究でのデータとして活用します。
【収集する項目】
患者さんの背景情報(年齢、性別、併存疾患、BMI、生活習慣)
血液検査データ(血算, プロトロンビン時間, Alb, AST, ALT, ALP, γGTP, T-Bil, BUN, Cre, CRP, NH3, 電解質,FBS, TG, T-chol, IgA,肝線維化マーカー(ヒアルロン酸 ,FIB4,APRI), Child-pugh スコア, MELDスコア,アルコール関連評価(DRL:飲酒量に基づくリスクレベル,HDD:多量飲酒日,TAC:総飲酒量), 予後スコア(Lille)、飲酒習慣スクリーニングテスト(AUDIT)
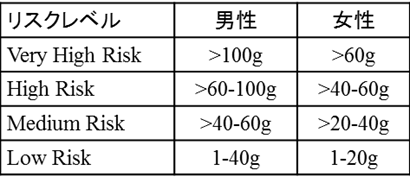
HDD:1日のアルコール消費量が男性60g超、女性40g超の1ヵ月あたりの日数(日/月)
TAC:1ヵ月あたりの平均アルコール消費量(g/日)
|
期間 |
内服時 |
内服後1か月 |
内服後3か月 |
内服後6か月 |
内服後12か月 |
|
同意 |
〇 |
|
|
|
|
|
患者背景 |
〇 |
|
|
|
|
|
血液検査 |
〇 |
〇 |
〇 |
〇 |
〇 |
|
Child-pugh スコア |
〇 |
〇 |
〇 |
〇 |
〇 |
|
MELDスコア |
〇 |
〇 |
〇 |
〇 |
〇 |
|
DRL |
〇 |
〇 |
〇 |
〇 |
〇 |
|
HDD |
〇 |
〇 |
〇 |
〇 |
〇 |
|
TAC |
〇 |
〇 |
〇 |
〇 |
〇 |
|
Lille |
〇 |
|
|
|
|
|
AUDIT |
〇 |
|
|
|
|
|
体重 |
〇 |
〇 |
〇 |
〇 |
〇 |
|
体組成・握力 |
〇 |
|
|
〇 |
〇 |
7. 研究機関、研究責任者
研究代表機関 :奈良県立医科大学附属病院
研究代表者:奈良県立医科大学 消化器・代謝内科 吉治 仁志
共同研究機関および研究責任者:別紙のとおり
8. 本研究で予測される利益、リスク
本研究は保険の適応内で行われる通常の診療の範囲内で行われますので、使用される薬剤、検査は参加される方の健康保険が適用されることになり、通常通りの自己負担になります。日常診療に比して、あなたが本研究に参加することで得られる特別な診療上、金銭的な利益はなく、特別な危険や不利益が生じることもありません。
9. 臨床研究の費用について
この研究で採用されている治療法、検査などは保険診療として認められており,通常の保険診療と同様の取り扱いとなりますので、本研究に参加することで得られる特別な診療上や金銭的な利益はありません。なお、ご参加いただくにあたっての謝金などのお支払いもありません。
10.同意しない場合でも不利益は受けません
この臨床研究への参加はあなたのご意思に基づくものですから、この臨床研究に同意なさらない場合でも不利益は受けません。従来の方法の中から適切と思われる方法を説明した上で選択しますので、今後の治療に支障はありません。
11.同意した後でもいつでも撤回できます
臨床研究を開始した後に、この臨床研究の継続を希望されない場合は、何時でも中止いたしますからお申し出ください。その場合でもあなたが不利益を受けることは一切ありません。
12.プライバシーは守られます
あなたのプライバシーに関することは第三者に漏れないよう充分配慮されています。あなたのプライバシーを守るため、診療録番号は研究対象者IDに変換し、あなたと研究対象者IDを結びつける対応表を用い管理します。この対応表は研究機関において厳重に保管されます。この臨床研究の研究成果を学会や学術雑誌に公表させていただくこともありますが、あなたの個人情報が公開されることはありません。また、この臨床研究が正しく行われているかを調査する目的で、奈良県立医科大学医の倫理審査委員会(臨床研究の計画を医学的立場と人道上の立場で検討する委員会)や厚生労働省関連機関などが、あなたのカルテなどを調べることもありますが、これらの関係者には守秘義務が課せられていますので、あなたのお名前などのプライバシーにかかわる情報は守られます。
またこの研究のデータを別の目的の研究に二次的に利用する場合もあります。その際は新たに研究計画書を作成し、別途倫理審査委員会の承認を受けて実施します。その場合もあなた個人を識別できるような情報がもれることはありません。
13.試料・情報の保存、廃棄の方法
期間中のデータは全てデータ管理責任者(研究責任者)が厳重に保管します。データベースには、個人情報の保護に配慮してあなたの氏名は使用せずに匿名化した研究対象者IDとして厳重に管理します。また、体から取得した情報等を廃棄する場合は、匿名化し、再現不可能な状態にして破棄します。データは、当該論文発表後5年間保管します。
14. 臨床研究に係る資金源、起こり得る利害の衝突
この臨床研究には、企業等との開示すべき重要な利害関係はありません
15. 臨床研究に関する情報の公開
本研究の結果は、学会発表や学術論文として報告する予定です。その際も、研究参加者個人が特定される情報は公開されません。
また、本研究の概要(研究の名称、目的、方法、実施体制等)は、大学病院医療情報ネットワーク「UMIN」に登録します。あなたが特定される情報は、登録しません。
URL: https://www.umin.ac.jp/
16. 倫理審査
本研究は、奈良県立医科大学医の倫理審査委員会で審査され、研究機関の長により承認されています。
17. 守っていただくこと
この臨床研究への参加に同意された場合、私(担当医師)の指示(例えば来院日、日常生活での注意事項など)を守っていただくことになります。このことにより、あなたがこの臨床研究に参加していただいて得られた貴重な成績が、今後の治療法に生かされることになります。
18. 相談窓口
あなたがこの臨床研究に同意することを決める前でも、同意した後でもこの臨床研究に関して知りたいことや心配なこと、分からないことがありましたら、下記の連絡先にお尋ねください。また、研究期間中、何か異常があれば、どんなことでもかまいませんので、直ちにお申し出ください。
連 絡 先 機関名:南奈良総合医療センター
担当者所属部署・氏名:消化器病センター(消化器内科) センター長 沢井正佳
電話番号: 0747-54-5000
E-mail:sawai-masayoshi@nanwairyou.jp
肝細胞癌に対するアテゾリブマブ+ベバシズマブ併用療法不応・不耐症例に対するLEN-TACE療法の有効性・安全性を評価する多施設共同観察研究 承認受付番号A5
これまでに切除不能肝細胞癌の治療を受けた患者さまへ
南奈良総合医療センター 消化器内科では、「肝細胞癌に対するアテゾリブマブ+ベバシズマブ 併用療法不応・不耐症例に対する LEN-TACE 療法 の有効性・安全性を評価する多施設共同観察研究」という臨床研究を実施しております。この研究は進行肝細胞癌に対する分子標的薬を用いた全身化学療法の有効性を調べることを主な目的としています。この臨床研究の概要についてご確認いただき、問い合わせなどがありましたら「問い合わせ先」へご照会ください。
この臨床研究は、奈良県立医科大学医の倫理審査委員会で審査され、研究機関の長の許可を得て行います。
【研究代表者】奈良県立医科大学付属病院消化器代謝内科 小泉 有利
【共同研究機関/責任者】
1. 奈良県総合医療センター 消化器内科 守屋 圭
2. 奈良県西和医療センター 消化器・糖尿病内科 吉田 太之
3. 南奈良総合医療センター 消化器内科 沢井 正佳
4. 大和高田市立病院 消化器内科 石田 光志
5. 済生会中和病院 消化器内科 上田 重彦
6. ベルランド総合病院 消化器内科 安 辰一
7. 医真会八尾総合病院 消化器センター内科 鶴薗 卓也
8. 近畿大学医学部奈良病院 消化器内科 川崎 俊彦
【研究の目的】
実臨床における肝細胞癌に対するアテゾリブマブ+ベバシズマブ併用療法不応・不耐症例に対するLEN-TACE療法の有効性を多施設共同で検証します。
【研究対象者】
切除不能肝細胞癌の患者さまで、1次薬物療法としてtezolizumab+Bevacizumab併用療法の治療歴があり、不応・不耐となった患者さまで、2次薬物療法としてレンバチニブの投与の適応があり、かつTACE可能な肝内病変が指摘されている患者さま。
上記条件に合致する患者さまで、2018年4月1日から2026年3月31日までにレンバチニブ+TACE治療(LEN-TACE療法)を受けられた方を対象とします。
【研究期間】
研究期間:実施許可日~2027年3月31日
【研究の方法】
切除不能肝細胞癌に対して、全身化学療法の投薬を受け治療された患者さんに対し、患者背景(性別や年齢、肝疾患の原因など)や腫瘍の大きさ・個数・腫瘍マーカーといった腫瘍に関する情報、肝機能などの血液データ、また投薬治療後の治療効果に関するデータを収集し解析します。(収集するデータは、治療開始前、治療開始後の評価時のデータが対象です。)
【個人情報の取扱い】
カルテIDや氏名などの個人情報を研究用IDに置きかえて使用するため、あなたの個人情報が外部へ漏れることはありません。カルテIDと研究IDの対応表は厳重に研究責任者において管理されます。
研究の成果は、学会や学術誌などで公表されますが、この場合も、個人が特定される情報が公開されることはありません。
【利益相反】利益相反とは、「主に経済的な利害関係によって公正かつ適正な判断が歪められてしまうこと、または、歪められているのではないかと疑われかねない事態」のことを指します。具体的には、製薬企業等から研究者へ提供される謝金や研究費等がこれにあたりますが、この研究は、特定の企業・団体等からの支援を得て実施するものではありません。
※ご希望があれば、他の研究対象者の個人情報保護に支障がない範囲内で、研究計画書および関連資料を閲覧することができますので、お申し出ください。
※この研究のカルテ情報使用についてご了承いただけない場合や、研究に対する問い合わせがありましたら、下記までご連絡ください。ご了承いただけない場合でも、今後の治療などに不利益を受けることはありません。
【問い合わせ先】
南奈良総合医療センター 消化器内科
研究責任者 沢井正佳
Tel:0747-54-5000
ファックス:0747-54-5020
e-mail:sawai-masayoshi@nanwairyou.jp
お問い合わせ
南和広域医療企業団南奈良総合医療センター診療部消化器内科
